CDMO服务
GMP级生产制备平台,先进治疗药品走向世界和商业化的桥梁
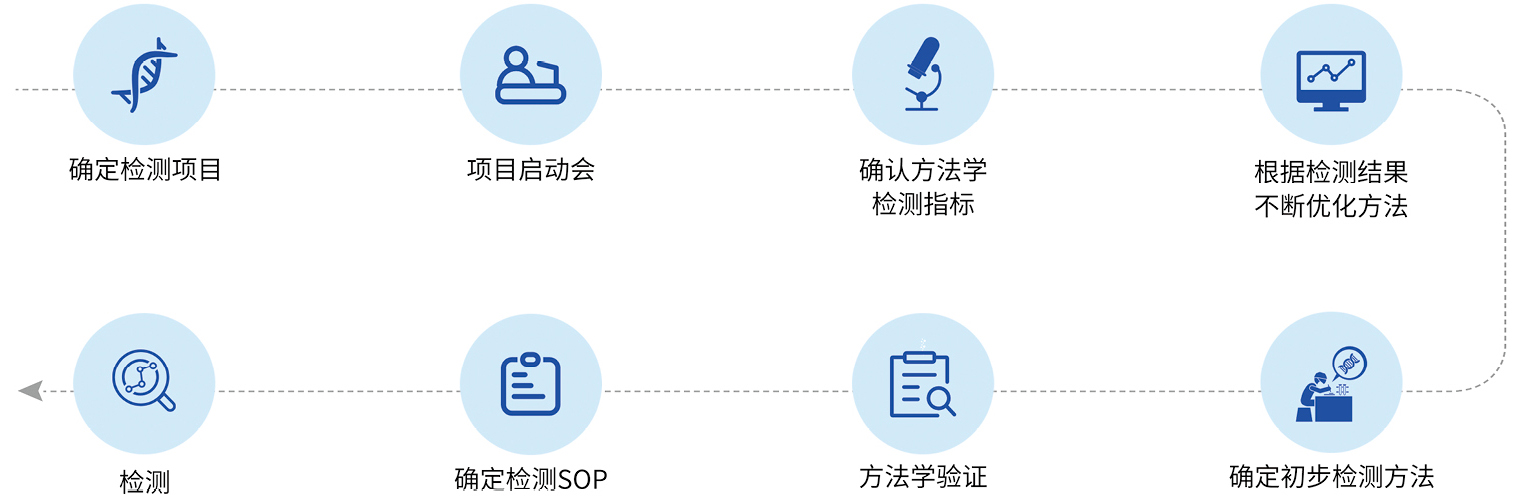
在细胞和基因疗法领域中,方法学验证必须遵守药典标准和监管要求,以确保产品的安全性、有效性和质量可控性。此外,方法学验证应针对治疗产品的特定特性进行定制,考虑其独特的作用机制和预期的临床应用。
| 参数(parameter) | 机构(organization) |
| 专属性(specifcily) | |
| USP, EP,ChP,ICH | |
| 精密度(precision) | |
| USP,EP,ChP,ICH | |
| 重复性(repeatability) | |
| ICH, ChP,ISO 17025 | |
| 中间精密度(intermediate precision) | |
| ICH, ChP | |
| 重现性(reproducibility) | |
| ICH, ChP, USP 和IS0 17025 | |
| 准确度(accuracy) | |
| USP,EP,ChP,ICH, ISO 17025 | |
| 线性(linearily) | |
| USP,EP,ChP,ICH,ISO 17025 | |
| 范围(range) | |
| USP, ChP,ICH | |
| 检测限(detection limil) | |
| USP,EP,ChP,ICH,ISO 17025 | |
| 定量限(quantitation limit) | |
| USP,EP,ChP,ICH,IS0 17025 | |
| 耐用性(robustness) | |
| USP,EP,ISO 17025 |