慢病毒载体(LVV)作为体外和体内CAR-T生产的主要平台,其产能和成本控制是LVV制造面临的主要挑战。宜明生物创造性研发搭建的Ubri-LVV TurboTM慢病毒载体生产平台,通过整合了293TH悬浮培养细胞系、全封闭下游处理系统、以及UltraCell™(与Syenex合作)+三大核心技术模块,实现了“产量倍增+成本锐减”的双重突破,助力技术快速转化。
依托全球的前瞻技术研发中心,宜明生物在慢病毒载体药物开发领域建立了强大的技术储备池,始终与全球前沿市场的技术保持同步。丰富生产和工艺开发经验,符合NMPA, FDA和EMA等相关法规要求的cGMP厂房设计,已成功帮助客户完成30+项IND项目获批进入临床,并成功交付多个批次病毒载体临床批生产订单。
60+批次GMP级慢病毒制备
GMP质量管理体系,支持中美IND项目注册申报
专业的生产和检测团队,确保产品高质量交付
定制化方法学开发与验证服务,满足项目的个性化需求
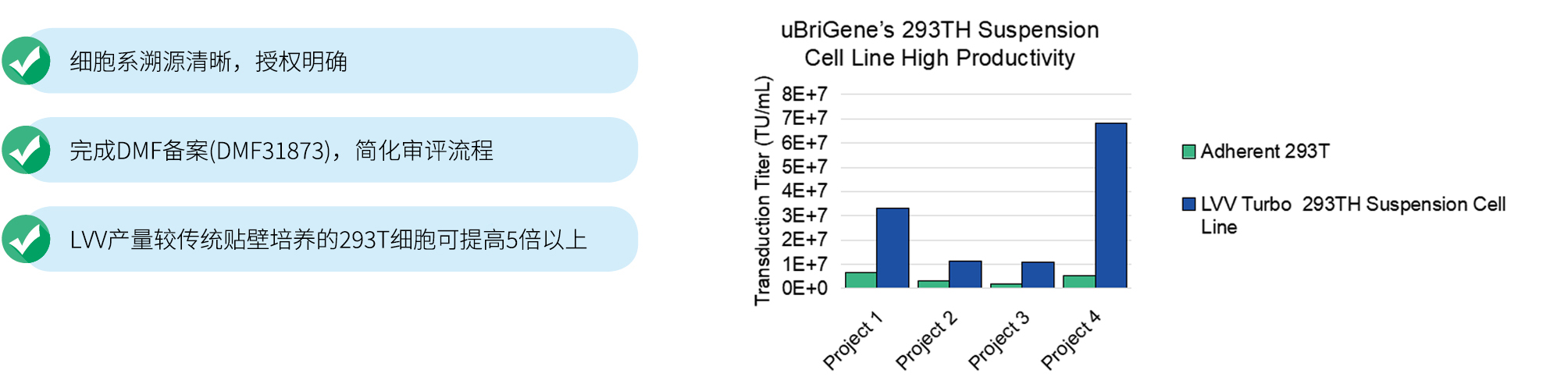

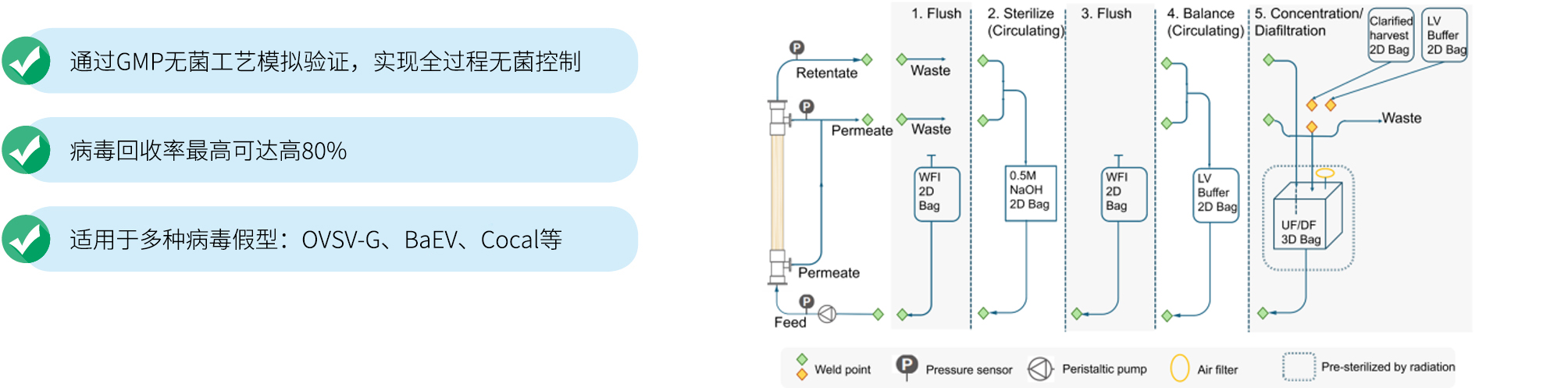
宜明生物的GMP慢病毒生产在C+A洁净车间进行。包括上游的细胞培养、质粒转染以及澄清等,下游的纯化、无菌灌装和储存。
宜明生物拥有专业的GMP质量控制团队,擅长方法学开发,可提供GMP级质粒、病毒载体及细胞治疗等产品的质量控制方案。宜明生物的质量控制平台涵盖了化学、微生物学、生物化学等方面的检测,可提供多种技术解决方案,助力客户开发、建立基因治疗产品的检测方法,满足所有GMP项目的检测要求。
| 检测项目 | 检验方法 | |
| 鉴别* | ||
| Sanger测序 | ||
| 物理检查 | ||
| 外观 | 目视法 | |
| 化学检定 | ||
| pH值 | pH值测定法 | |
| 总颗粒数(p24) | ELISA | |
| 比活性(按客户需求) | / | |
| 慢病毒转导滴度(按客户实际情况) | / | |
| 纯度 | ||
| 宿主DNA残留 | qPCR | |
| 纯度 | ||
| 质粒DNA残留 | qPCR | |
| 外源DNA片段大小 | 毛细管电泳 | |
| 宿主蛋白残留 | ELISA | |
| 核酸酶残留 | ELISA | |
| 牛血清白蛋白残留 | ELISA | |
| SV40基因残留 | qPCR法 | |
| E1A基因残留 | qPCR法 | |
| 安全性 | ||
| 内毒素 | 凝胶限度试验(凝胶法) | |
| 无菌检查 | 直接接种法 | |
| 支原体 | PCR/qPCR | |
| RCL检测(EOPC&UPB)* | 培养法 |
宜明生物组建了高效的项目管理团队,完善的项目沟通机制和全方面的IP保护,确保每一个CDMO项目的高质量实施交付。
项目管理团队
专业的项目管理团队
对客户需求及时响应
项目沟通机制
定期例会汇报项目进度
线上现场多渠道高效沟通
全方位IP保护
安全的信息加密系统
企业内部项目代码管理
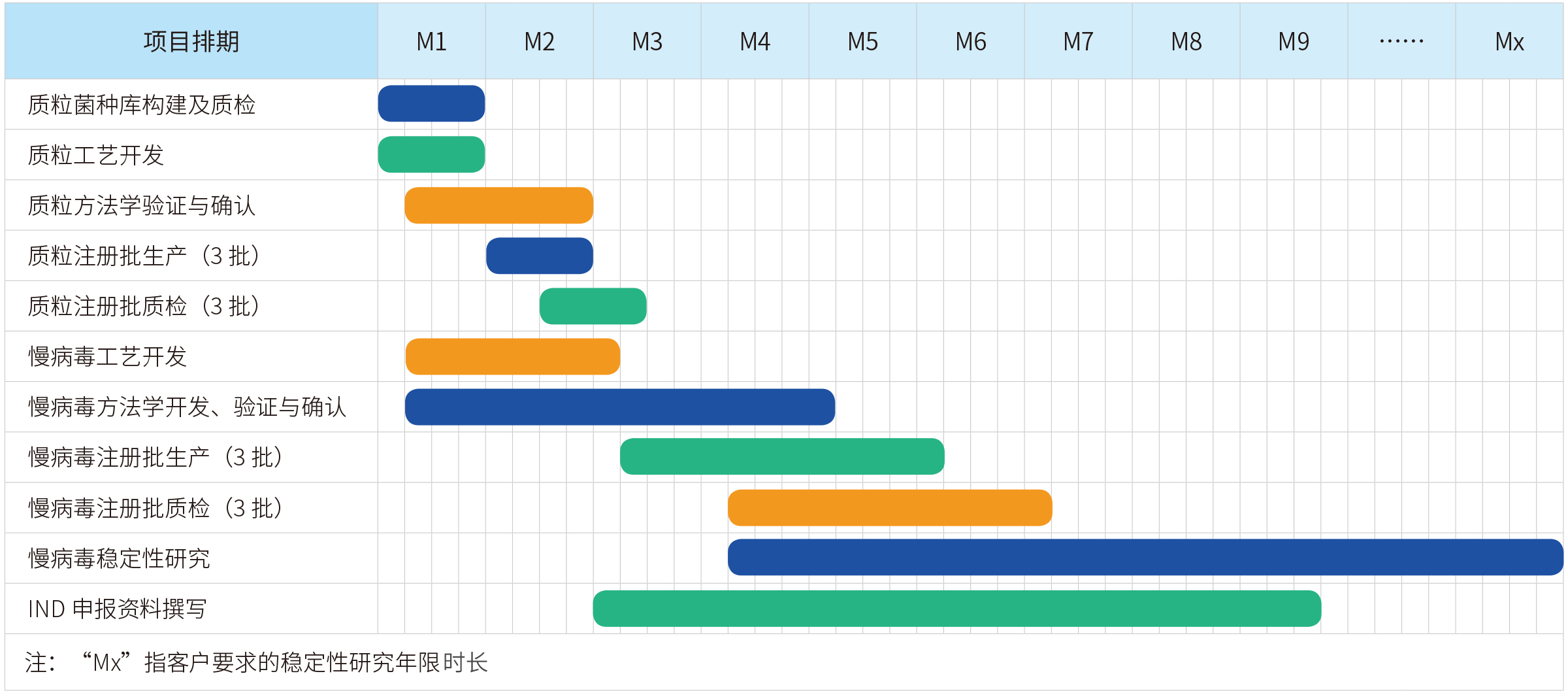
宜明生物建立了成熟的病毒载体工艺平台,丰富的项目经验确保可以实现快速的开发生产流程,为客户提供完整的临床级IND项目服务,包括细胞库建库、工艺开发、方法学开发、稳定性研究,中试批生产等,亦可以根据项目需求提供定制服务。另外,为满足IND申报的要求,还可提供临床级慢病毒批生产记录、批检验记录以及相关验证资料等。
在TFF过程中,选择适合的材料和孔径的中空纤维或膜包,以实现病毒截留和杂质去除。优化TFF过程中的流速和跨膜压,以获得高得率。对于AEX工艺,首先需要选择合适的填料,能够完成病毒的捕获和有效的洗脱,其次需要调节冲洗的强度从而最大程度的去除杂质。
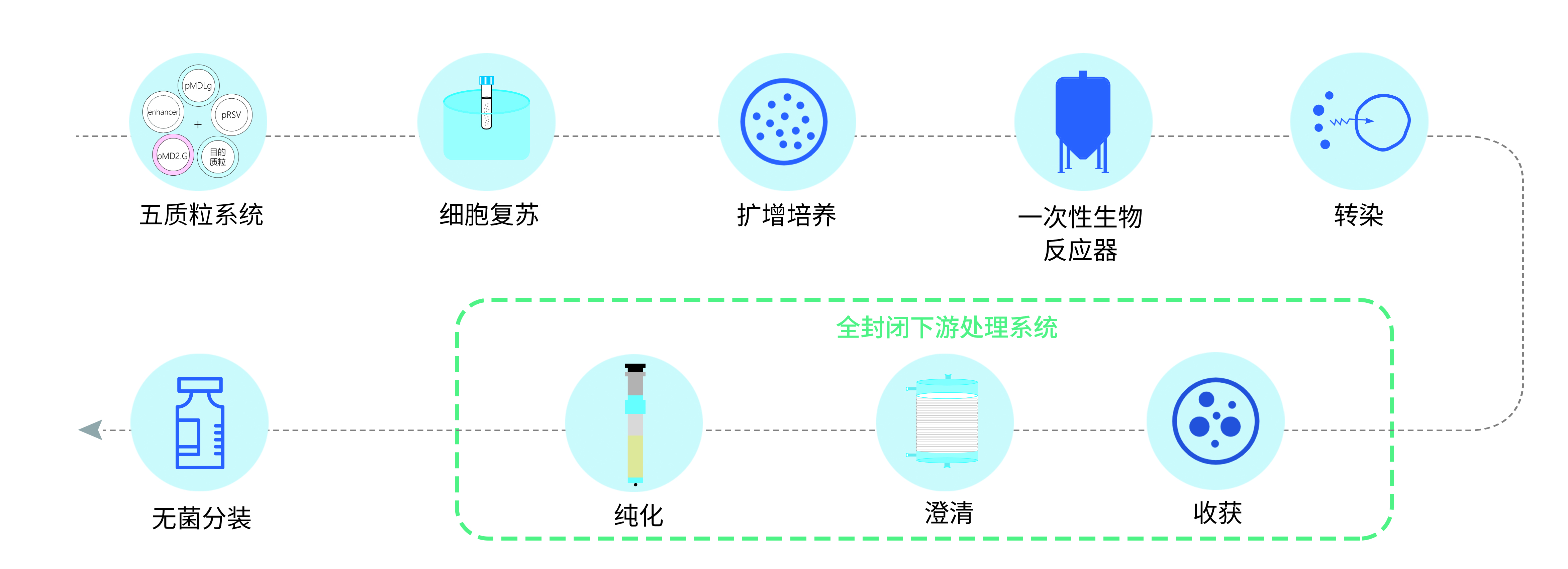
宜明生物的GMP慢病毒生产在C+A洁净车间进行。包括上游的细胞培养、质粒转染以及澄清等,下游的纯化、无菌灌装和储存。大部分工序在封闭体系中进行(如生物反应器,一次性生物反应罐等)
作为表征研究,由于慢病毒载体的本身复杂性,进行选用多种方法,从不同维度,orthogonal的来获取相对全面的质量特性。
虽然目前指导原则不要求同时研究病毒载体和整合后序列,但这是可以进一步完善的。整合后序列数据有助于更好理解序列变体的形态和风险。

