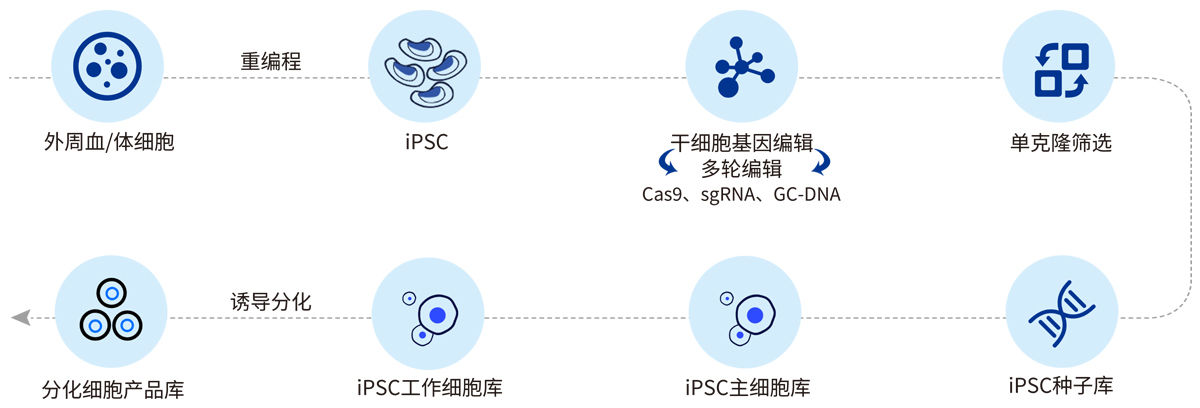
iPSC的发现为医学界带来了新的视角和福音,而通过iPSC技术与CRISPR/Cas9基因编辑技术联用,可以实现个性化治疗,更是开启了疾病治疗的新篇章。宜明生物开发并建立完善的GMP iPSC重编程工艺平台,并可提供GMP级别的基因编辑元件生产(cas9/mRNA、dsDNA、sgRNA)以及iPSC细胞建库一站式服务。专有的创新技术在显著提高元件稳定性的同时,其简化的制备工艺还可大幅度降低商业化生产成本,让创新成果惠及更多患者。
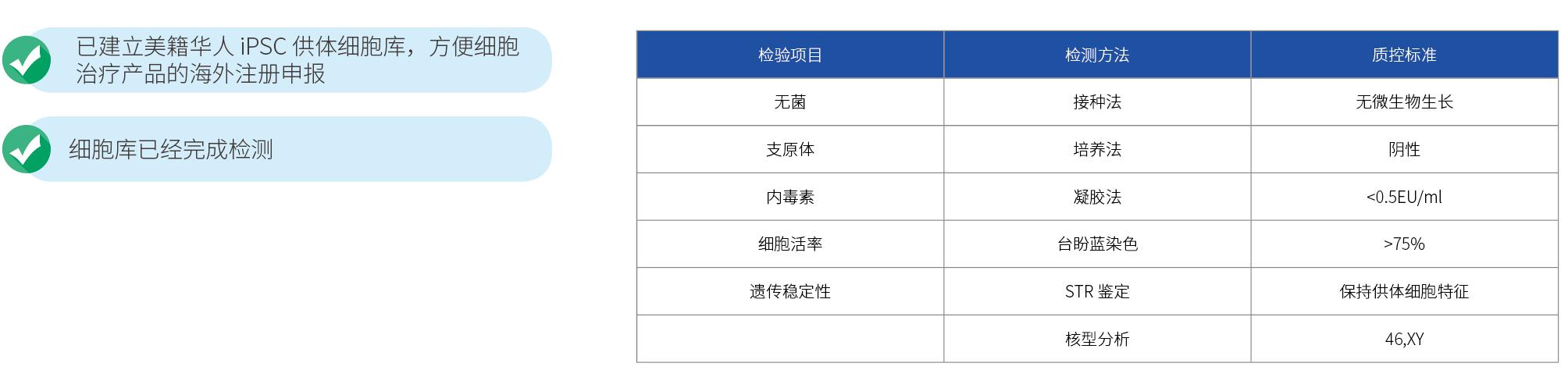
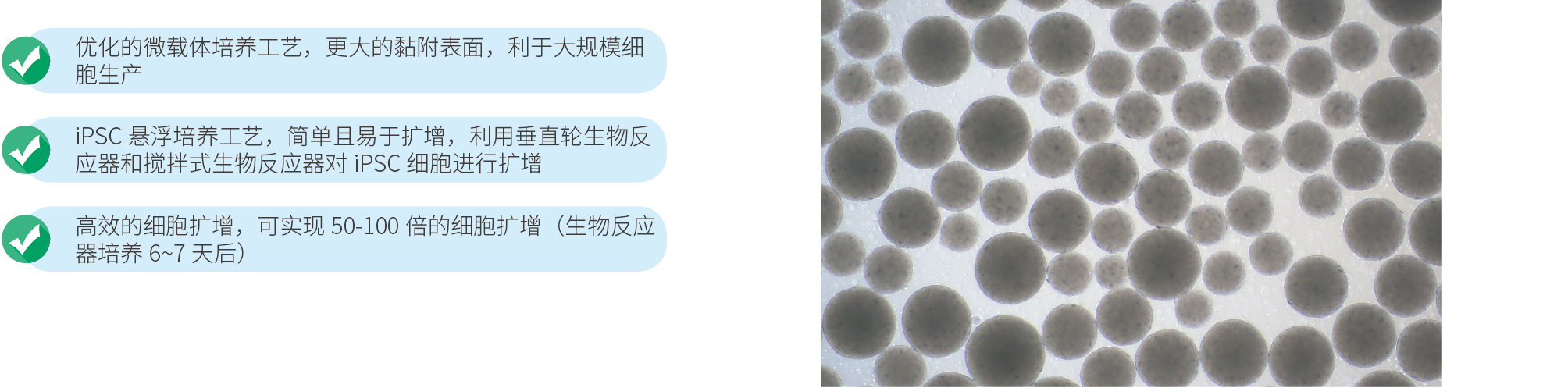
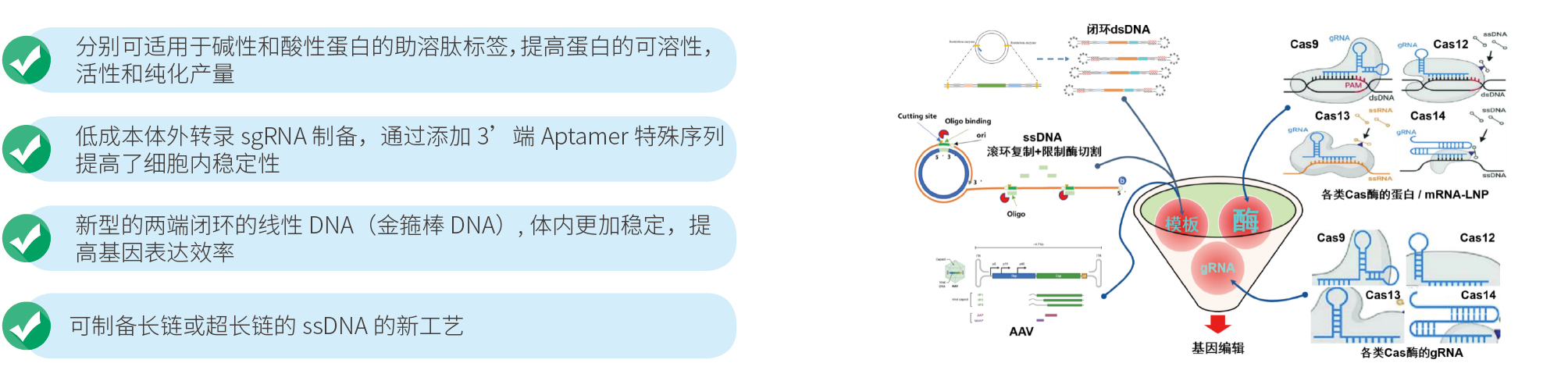
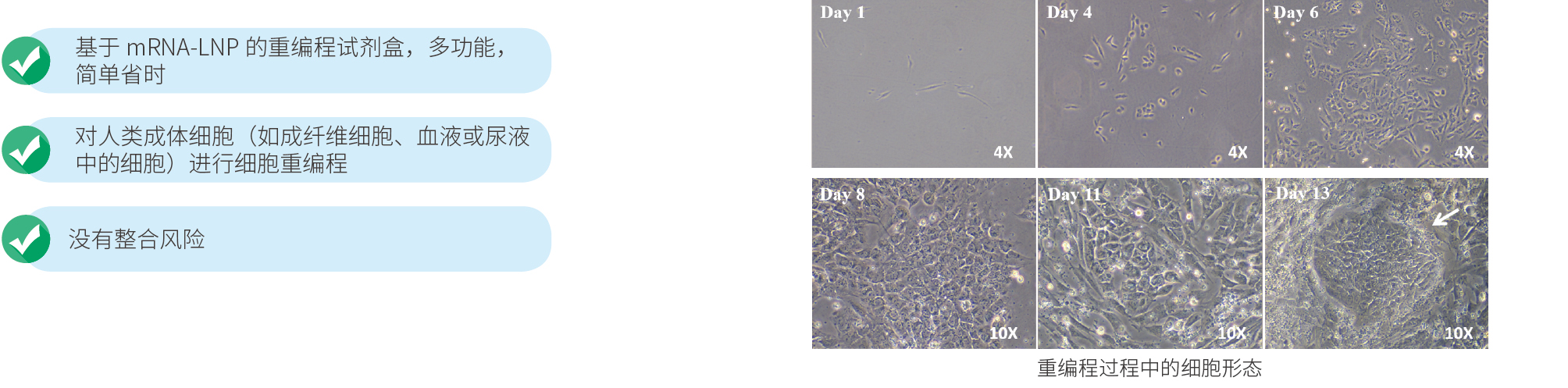
宜明生物拥有丰富的基因编辑和细胞治疗产品的开发及生产经验,iPSC的制备为绝对A级全封闭隔离器生产环境,一次性生产工艺避免了交叉污染。
宜明生物拥有专业的GMP质量控制团队,擅长方法学开发,可提供GMP级细胞治疗产品的质量控制方案。宜明生物的质量控制平台涵盖了化学、微生物学、生物化学等方面的检测,可提供多种技术解决方案,助力客户开发、建立细胞治疗产品的检测方法,满足所有GMP项目的检测要求。
| MCB | WCB | EOPC | UPB | UPB | UPB | ||
| 无菌 | |||||||
| 检验 | + | + | + | + 微生物限度 | + 微生物限度 | + 微生物限度 | |
| 方法适用性 | + | - | + | - | + | - | |
| 支原体 | |||||||
| 检验 | + | + | + | + | + | + | |
| 方法适用性 | usp+ | - | usp+ | - | usp+ | - | |
| 分枝杆菌* | |||||||
| + | + | + | - | - | - | ||
| 细胞内外源因子检查 | |||||||
| 细胞形态观察及血吸附试验* | + | + | + | - | - | - | |
| 体外不同细胞接种法* | + | + | + | + | + | + | |
| 动物和鸡胚体内接种法* | + | - | + | - | + | - | |
| 逆转录酶活性检查 * | + | - | + | - | - | - | |
| 逆转录病毒检查-透射电镜观察* | + | - | + | + | + | + | |
| 逆转录病毒检查-感染性试验* | + | - | + | - | - | - | |
| 人源性病毒 | + | - | - | - | - | - | |
| 牛源性病毒* | + | - | - | - | - | - | |
| 猪源性病毒* | |||||||
| + | - | - | - | - | - | - | |
| 鼠细小病毒(MVM)* | + | - | + | + | + | + |
宜明生物组建了高效的项目管理团队,完善的项目沟通机制和全方面的IP保护,确保每一个CDMO项目的高质量实施交付。
项目管理团队
专业的项目管理团队
对客户需求及时响应
项目沟通机制
定期例会汇报项目进度
线上现场多渠道高效沟通
全方位IP保护
安全的信息加密系统
企业内部项目代码管理
宜明生物建立了成熟的iPSC工艺平台,丰富的项目经验确保可以实现快速的项目交付,为客户提供完整的临床级IND项目服务,包括细胞库建库、工艺开发、方法学开发、稳定性研究等,亦可以根据项目需求提供定制服务。另外,为满足IND申报的要求,还可提供临床级iPSC细胞库批生产记录、批检验记录以及相关验证资料等。

1) 细胞来源 :细胞来源于可无限增殖的iPSC种子细胞,传统细胞治疗来源于患者或健康人;
2)基因编辑:易于改造且改造完全(基因编辑);传统细胞治疗随机插入,效率更低(慢病毒感染);
3)细胞特征:iPSC细胞来源于同一个种子细胞,细胞类型均一,特征明确;
4)产量、成本:免疫排斥低,更容易异体使用,可批量生产,因而成本更低。
需要建二级库MCB/WCB;法规无具体支数要求MCB建议100支,WCB建议500支;每支一般需要1-5E6细胞/支(与适应症有关);代次次数没要求,需要覆盖以后生产实际的代次。
我们提供可定制生产服务,以满足特定的研究或治疗需求。包括选择供体细胞、优化重编程方案以及根据项目要求表征细胞系等服务。
生产周期可能因项目的复杂性和规模而异。一般iPSC 生产需要几周到几个月的时间
宜明生物可提供全面的细胞治疗服务,包括 iPSC 生产、工艺开发、细胞库、质量控制和注册申报等一站式CDMO服务。

