腺相关病毒(Adeno-associated virus, AAV)是基因治疗领域最受欢迎的病毒载体之一。然而AAV药物因其较大的分子尺寸、复杂的结构、异质性以及有限的样本量,使得分析表征这类产品非常具有挑战性。 质谱(Mass spectrometry,MS)是AAV的关键分析工具之一,可以在AAV开发过程中直接、准确地评估AAV产品的质量。早期,人们尝试使用傅里叶变换离子回旋共振质谱来表征衣壳蛋白的糖基化,以及四极杆飞行时间质谱法(QTOF)来鉴定不同AAV的血清型。目前的AAV研究采用更复杂的质谱技术(如原生质谱和电荷检测质谱)分析完整的AAV,采用基于质谱的肽图谱并结合蛋白质组学表征衣壳蛋白和鉴定工艺杂质。本文将重点介绍质谱在完整AAV分析、衣壳蛋白表征和杂质分析中的应用。
完整AAV载体分析
对于AAV基因疗法来说,“基因组正确包装”是其生产的关键点。监管部门也将基因组包装和组装一致性的测试作为原料药表征的一部分。目前AAV载体的主要分析检测方法包括:应用分析超速离心(AUC)和电子显微镜(EM)来区分和定量各衣壳亚群;用基于PCR的方法确定基因组滴度;用于基于酶联免疫吸附测定(ELISA)的方法定量衣壳滴度。然而,这些方法有一定的局限性,如需要大量的样本(AUC),人工检查和计数(EM),低通量(AUC和EM)以及无法同时检测衣壳及其包装的基因“货物”(PCR和ELISA)。
质谱分析是通过测定待测样品的离子质荷比(mass-to-charge-ratio)来进行分析的方法。多年来,质谱已被用于复杂的生物大分子的结构表征。作为一种分析完整AAV载体的替代工具,MS具有所需样品量小、分析速度快、灵敏度高、动态范围大和质量分辨率高等优点,可以区分完整衣壳、部分衣壳和空衣壳亚群。下面主要介绍原生质谱(Native MS)和电荷检测质谱(CDMS)。
1、原生质谱
原生质谱与EM方法不同,后者涉及染色和干燥等步骤,可能会破坏病毒颗粒的完整性,而原生质谱是在病毒颗粒的天然状态下进行分析,可获得更准确的数据。目前已有多项研究证实了原生质谱测定病毒完整质量的能力(见图一)。有人获得了HBV衣壳两种结构形式的33个质谱,高质量分辨率能够精确地测定各自在3 MDa和4 MDa的质量。还有研究者应用改造后的Orbitrap质谱仪,成功地估算出组成AAV1衣壳的三种病毒蛋白(VP1, VP2, VP3)的化学计量。
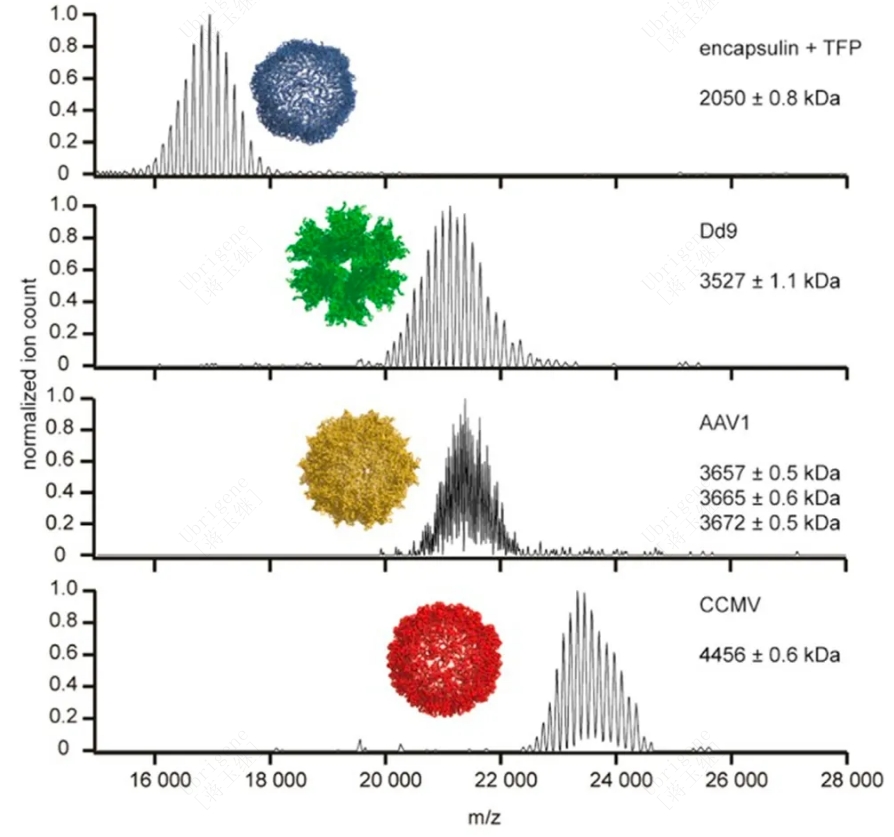
图一|不同病毒样颗粒的原生质谱及其相应的结构和平均反卷积质量(±标准差);(数据来源:doi.org/10.1016/j.drudis.2022.103442)
原生质谱法可以检测完整衣壳、部分衣壳以及空衣壳的相对水平,这是AAV制备的一个关键质量属性,因为空衣壳/部分衣壳会引发不必要的免疫反应,降低转导效率,最终降低基因治疗产品的功效。
原生质谱法耗时短,样品制备简易,所需样品量少,与AUC、色谱法、EM和基于UV吸光度的检测方法相比具有明显的优势。有研究证实将原生纳米电喷雾电泳迁移率分子分析仪与原生质谱结合,可以区分包含或缺失单链DNA的AAV8颗粒。还有人在自然条件下使用direct-infusion MS可以快速确定AAV5和AAV8.43的空衣壳与完整衣壳的比例。
原生质谱需要通过分辨电喷雾电离产生的不同电荷状态以测量质量。然而AAV病毒颗粒包装的“基因组货物“长短/数量不一,这一非均质性使得相邻电荷态的质谱信号重叠,导致质谱分辨率低。这也是AAV载体的原生质谱分析的主要挑战之一。
2、电荷检测质谱法(CDMS)
CDMS是通过同时测量单个离子的质荷比和电荷数,进而算得离子质量的单粒子统计方法,在测定超大分子离子的质量分布方面有独特的优势,可用于分析包装了基因组货物的病毒衣壳(见图二)。飞行时间(TOF)和线性离子阱(linear ion traps )是CDMS中较常用的质谱分析仪。基于Orbitrap(一种离子阱质量分析仪)的CDMS可以在短时间内(<30分钟)以极少量(丰度低于2%)的AAV样品(ul)即可实现精确的质量测定和AAV颗粒亚群的测定。
如图二所示CDMS可以准确区分完整衣壳,部分衣壳以及空衣壳。图二a中3.7 MDa的峰值与空衣壳的预期质量接近,5.1 MDa的峰值是包装了完整基因组的衣壳。这两个主要峰之间的1.4 MDa质量差与所包装的scGFP基因组质量(1.389 MDa)一致。根据图2a所示,35%是空衣壳,23%是完整衣壳,42%是部分衣壳。通过CDMS确定每个亚群的相对比例与EM的手动图像计数(图二b)所获得的百分比相当,且变异性较小。
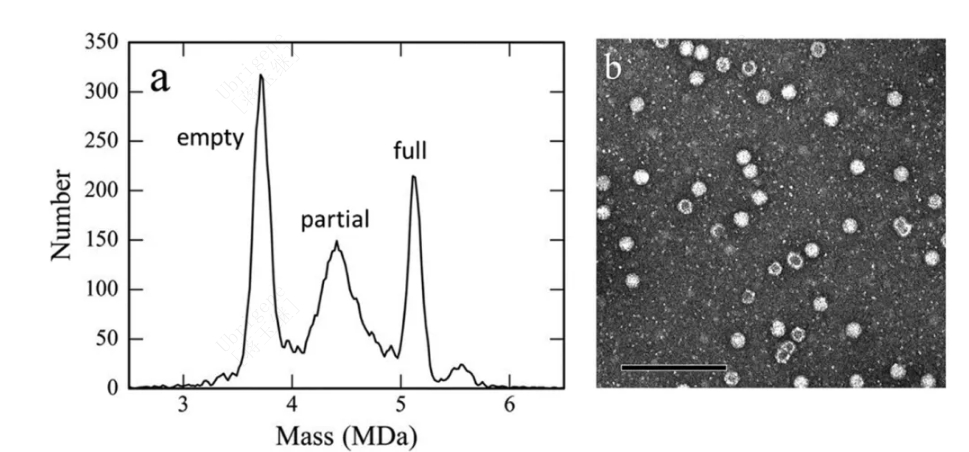
图二|a)包装scGFP基因组的AAV8质量直方图,b)同一样品的EM数据(比例尺= 200 nm);(数据来源:doi.org/10.1016/j.drudis.2022.103442)
CDMS在定量空衣壳/完整衣壳比例方面的精确度与AUC相当,CDMS还可以准确地测量各衣壳亚群的分子量,并根据完整衣壳和空衣壳之间的质量差来估算所包装的基因组大小。此外,CDMS检测仅需少量样品。尽管优势明显,CDMS对仪器的要求更高,需要更复杂的技术和专业知识。
衣壳蛋白的表征
完整的AAV病毒的表征固然重要,但是监管部门还要求表征AAV病毒的“结构和其他特征”。目前行业内主要采用基于PCR的方法鉴定病毒基因组成分。对于AAV VP(viral protein)组分,不仅需要在完整的蛋白水平上进行表征,还要确定其氨基酸序列(血清型)、初级结构和PTM分析。质谱技术具有独特的分析特性,还可与其他分离技术相结合,有望成为表征AAV VP的首选方法。
1、AAV血清型鉴定
AAV血清型的鉴定主要基于衣壳VPs。不同血清型AAV的组织趋向性、转导效率、效力和安全性各有不同,但是其VP序列却很接近。基于ELISA的鉴定方法需要开发血清型特异性抗体来识别特定的衣壳表位,而且对于高度相似的血清型,这类方法可能会因交叉反应而存在特异性问题。基于衣壳热稳定性的差示扫描荧光法(DSF)是近年来发展起来的一种简单、快速的AAV血清型鉴别方法,但其分辨率不高,很难区分熔解温度相似的血清型。
质谱与液相色谱(LC)结合可以直接分析来自不同AAV血清型的完整衣壳蛋白。质谱还可以与多种分离平台结合,如反相液相色谱(RPLC),亲水相互作用色谱(HILIC), 2D液相色谱(2DLC和毛细管电泳(CE),通过这些方法在质谱分析前有效地分离VP成分。
肽图谱分析也是血清型鉴定的重要工具。应用酶消化目标蛋白而产生的一组肽片段,是蛋白氨基酸序列的独特“图谱”。每个肽通过串联质谱(MS/MS)进行色谱分离和测序,用于蛋白ID的鉴定。此外,肽图谱也能够区分野生型AAV和突变型AAV。
2、确定VP比率
AAV衣壳是由VP1, VP2, VP3组合的60个亚基的二十面体。在AAV的生产过程中,VP1:VP2:VP3化学计量的相对比例对于载体的效力、传染性和转导效率至关重要。质谱与液相色谱及毛细血管电泳联用可准确检测VP比率。用质谱估测VP比率的同时还可以表征每个VP的分子量以及PTMs等。
3、初级结构及PTM分析
阐明AAV原料药的主要结构和与产品相关的变异是AAV原料药表征的基本要求。完整质量结合质谱多肽图谱已成为确定蛋白ID的常用方法。此外,还可以根据根据完整质量分析中的分子大小和质量分辨率推断蛋白质一级结构的变化,如剪切和修饰(如乙酰化、氧化和磷酸化),也可以探测蛋白PTM的存在和相对水平。
肽图谱可以提供修饰残基的特异性定位。根据肽图谱数据,人们已经在AAV中发现了几种PTMs,包括脱酰胺、氧化、异构化、糖基化、磷酸化、SUMO化、泛素化和乙酰化。表征AAV中的PTM使我们更好地了解其生物学相关性和影响。例如,AAV8表面暴露的天冬酰胺残基的脱酰胺与转导效率的损失相关;AAV9中特定天冬酰胺残基的脱酰胺与T细胞介导的免疫反应相关;AAV2的点突变结果表明,一个特定的糖基化位点可能对包装很重要,而一个SUMO化位点可能对转导很重要。可见质谱在这类结构-功能关系研究是重要的。
杂质分析
原料药生产过程中的残留杂质包括残留的宿主细胞蛋白、空衣壳、外来核酸序列和与工艺相关的杂质(如生产过程中使用的残留试剂)。杂质的残留不仅影响药品的纯度、质量和疗效外,也是巨大的安全隐患。因此就需要灵敏的方法来检测。
1、宿主细胞蛋白(HCPs )
HCPs是可以与AAV载体共纯化的一类主要工艺杂质。 一些HCPs,即使是极少量,也会导致不必要的免疫原性效应和/或生物活性,从而降解药物,影响药物的滴度和效力。基于质谱的蛋白质组学方法可作为ELISA, western blotting和凝胶法的补充,用于鉴定和定量HCPs。比如,应用 LC-MS/MS分析消化SDS-PAGE凝胶带的蛋白质可用于检测和鉴定与衣壳VPs共纯化的蛋白质。应用基于LC-MS/MS蛋白质组学分析,通过对人HEK293和Sf9昆虫细胞制备的AAV载体中的HCPs进行比较分析,发现两者的差异(如Sf9制备的载体中存在潜在免疫原性N-糖基化HCPs)。
研究人员对HCPs进行了一项调查,通过LC-MS/MS蛋白组学鉴定了44种AAV相关的细胞蛋白, 并发现其中的一种Y-box结合蛋白(YB1)影响AAV载体的基因组滴度。并利用这一信息,他们建立了一种新的YB1 knockdown表达细胞系,该细胞系将载体基因组滴度提高45倍。因此通过分析基于MS的HCP蛋白质组学数据,可以更深刻理解AAV的制造过程并指导AAV生产的改进。
2、外源性核酸杂质
在AAV的制造过程中,核酸残留(包括宿主细胞DNA、质粒DNA和截短的载体DNA等)是常见的工艺相关杂质,导致AAV制剂的异质性。质谱可作为凝胶电泳和PCR法的一种正交方法来表征病毒载体中封装的基因货物。
虽然目前基于PCR的方法,如QPCR和ddPCR,是检测全基因组效价的行业标准方法,但若引物的目标序列被剪接出来,就无法检测出这部分截短基因组的存在。
CDMS则有可能可以弥补这一局限。CDMS不仅可以分析出AAV所包装的基因组不同的长度,可以利用完整衣壳与空衣壳的质量差来推断所包装的基因组的质量分布,还能够检测到包装了多个基因组拷贝的颗粒。
3、残留的试剂
残留试剂指AAV生产和纯化过程中使用的试剂残留,以及从柱子或其他生产材料中浸出的物质。质谱是基于被测分子的m/z,在保证样品的正确制备以及有效电离的前提下,质谱方法可以广泛应用于任何残留小分子杂质的检测。
以碘二醇为例(在密度梯度超离心法纯化AAV中的常见试剂),少量的碘二醇残留就可能引起过敏等不良反应。LC-MS可以灵敏可靠地检测量化AAV制剂中碘二醇残留,灵敏度可低至0.01 lg/ ml,可测量的线性范围达4个数量级。

